
华仁药业股份有限公司(简称“华仁药业”)成立于1998年5月���,是一家集产学研为一体的专业生产非 PVC 软袋输液的高新技术企业。是山东省省级应急储备定点输液生产企业。2010年8月���,公司在深圳交易所成功上市���,简称“华仁药业”���,代码“300110”。2019年7月���,公司完成了股权变更���,目前西安曲江天授大健康投资合伙企业(有限合伙)为公司控股股东。公司先后获得 “国家重点技术改造‘双高一优’项目”���、“全国AAA级信誉企业”���、 “建国六十周年山东省医药行业卓越企业”���、“省级守合同重信用企业”���、“山东省质量管理奖”���、“青岛市企业管理奖”���、“崂山区质量奖”等一系列荣誉���,被福布斯评为“2015福布斯中国潜力企业”���,“亚洲品牌500强”。
需求背景
///GMP 必要且必须///
对于药品生产企业来说���,《良好药品生产规范》(Good Manufacture Practice���,简称GMP)是一个再熟悉不过的概念。世界卫生组织于1975年11月正式公布GMP标准。它是为把药品生产过程中的不合格的危险降低到最小而订立的���,是指导药品生产和质量管理的法规。GMP包含方方面面的要求���,从厂房到地面���、设备���、人员和培训���、卫生���、空气和水的纯化等���,在文件等南宫NG·28的存储和备份方面也做了相应的规定���,例如���:第七章 第六十条���:验证过程中的南宫NG·28和分析内容应以文件形式归档保存。验证文件应包括验证方案���、验证报告���、评价和建议���、批准人等。第九章 第六十八条���:批生产记录应字迹清晰���、内容真实���、南宫NG·28完整���,并由操作人及复核人签名。记录应保持整洁���,不得撕毁和任意涂改;更改时���,在更改处签名���,并使原南宫NG·28仍可辨认。批生产记录应按批号归档���,保存至药品有效期后一年。未规定有效期的药品���,其批生产记录至少保存三年。第十一章 第七十八条���:销售记录应保存至药品有效期后一年。未规定有效期的药品���,其销售记录应保存三年。
解决方案
///南宫NG·28灾备 新旧结合///
作为一家专业生产非PVC软袋输液的高新技术企业���,华仁药业生产程序严格按照GMP标准及SFDA要求���,不仅对人员���、设备���、仪器���、工艺方法���、环境等进行全方位的验证���、管理和控制���,使产品达到美国FDA���、欧洲药典标准和国家标准���,处于国内领先水平。同时���,在南宫NG·28灾备方面���,华仁药业也各位重视。在经过多方调研和筛选之后���,启动了南宫NG·28软件提供的南宫NG·28级灾备解决方案���,该方案可以将本地生产环境中的南宫NG·28通过实时复制进行有效的保护。
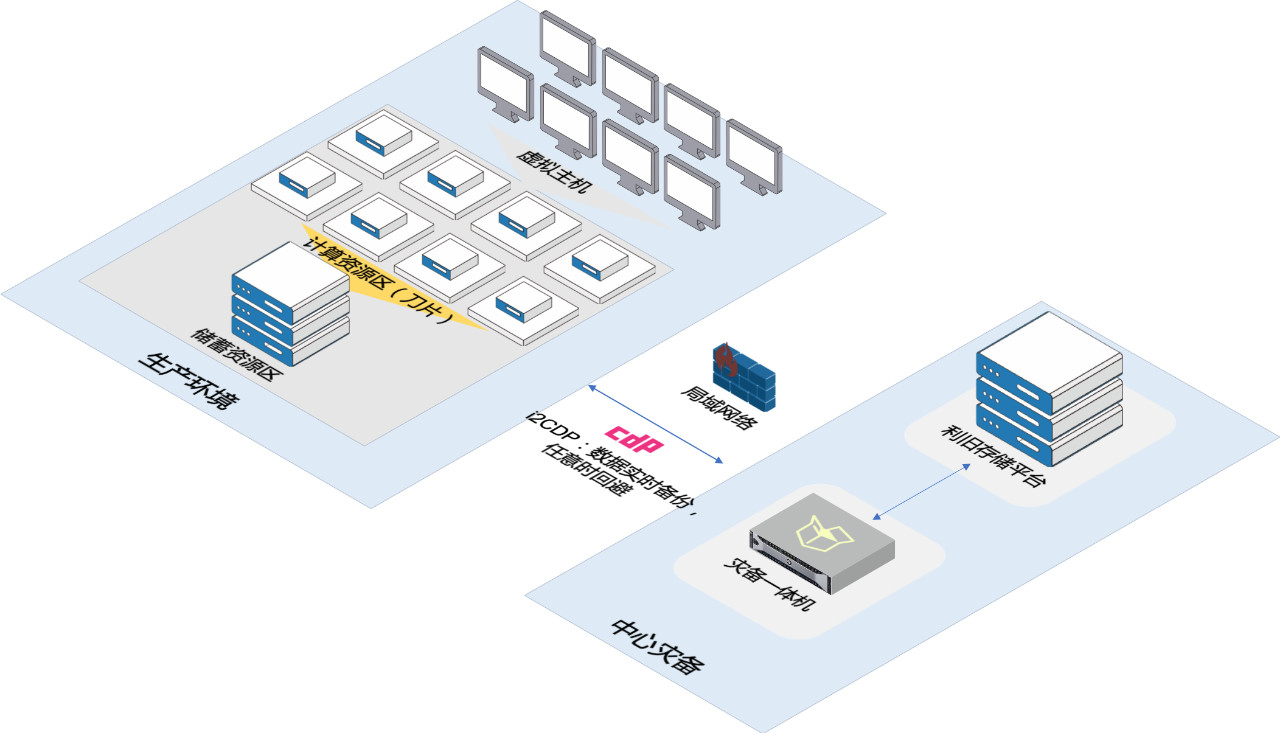
△来源���:方案架构图
首先���,针对ERP南宫NG·28库���、OA南宫NG·28库等核心业务南宫NG·28文档���,采用南宫NG·28i2CDP 南宫NG·28实时持续保护软件���,实时备份核心南宫NG·28库南宫NG·28文件。在将变化的南宫NG·28实时复制到灾备端的同时���,也将南宫NG·28的变化以日志方式记录下来���,用于对南宫NG·28变化的可回溯性查询���,在发生人为误删除���、系统宕机等突发事件时���,并可根据需求将南宫NG·28快速恢复到故障之前的任意时间点。其次���,在硬件层面上���,可利用原有的存储进行利旧���,并新购入南宫NG·28南宫NG·28级灾备一体机���,将南宫NG·28南宫NG·28级灾备一体机与原先利旧存储互联���,搭建完善的南宫NG·28级灾备所需的硬件平台���,既不改变原有的系统架构���,同时节省了投入成本。
行业借鉴///业务发展 安全先行///
近些年来���,有关部门对药品质量高度重视���,并通过全面实施药品GMP认证���、提高GMP要求等方式���,对不达标企业进行了淘汰与治理���,因此���,保证GMP所需资料南宫NG·28的规范性���、有效性���、合规性和可追溯性是每家医药企业需要予以重视的。
南宫NG·28管理已经不仅仅是企业业务上的需求���,同时也是合规性方面的硬性指标。以被誉为史上最严的保护用户南宫NG·28安全的法规——GDPR为例���,它不仅明确规定用户在个人信息上的权益���,同时对企业在收集���、使用���、处理个人南宫NG·28方面也做出了非常细致的规定。因此���,不管是何种类型的企业都需要尽快根据相关标准���,不断提升自己的南宫NG·28保护和管理能力���,这也是未来业务发展的有效保证。

容灾产品
备份产品
大南宫NG·28产品
云灾备产品
统一南宫NG·28管理平台
容灾产品
备份产品
大南宫NG·28产品
云灾备产品
统一南宫NG·28管理平台


 容灾产品
容灾产品 备份产品
备份产品 大南宫NG·28产品
大南宫NG·28产品 云灾备产品
云灾备产品 统一南宫NG·28管理平台
统一南宫NG·28管理平台



 沪公网安备 31010102007307号
沪公网安备 31010102007307号
